5月17日,捷信医药团队和活动嘉宾,和铂医药药物警戒总监 蓝丽丽女士一同庆祝了ePConnect™ - AE的功能上线。

近年来,随着药品上市持有人制度的落地,相关部门对上市后药物的安全性监测提出了新的要求:
-
卫生部81号文规定药品再注册时需要提交销售五年来临床使用及不良反应情况的总结报告,这个对于新药的再注册至关重要。
-
同时,2013年药监局颁布的“生产企业重点监测工作指南” 推荐采用前瞻性研究收集数据并对重点监测做了具体的指导,建议制药企业主动收集不低于3000例的药品使用的安全性数据。
-
另外,卫生部66号文也规定了药品上市持有人要加强药品不良反应的监测和分析。
捷信的ePConnect™ - AE功能模块是以ePRO(电子患者临床结局) 为基础,符合FDA Title21 CRF Part 11和CDISC标准,具有临床试验级别的患者隐私保护。
此产品可以很大地贴合AE数据收集的多种情境模式:
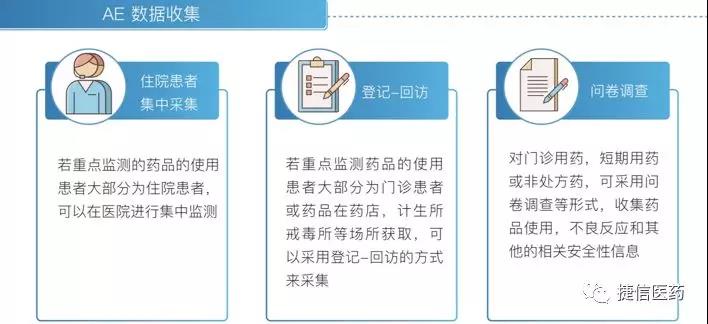
ePConnect™通过手机移动端工具来记录患者的不良反应报告,在过程中辅以定制化的患者教育内容,个体化的信息推送和服药记录,能够真正个体化地为患者创造价值并提供更个体化的疾病管理,帮助药企大大提升了患者在此类数据收集项目中的参与动力,和患者的实际用药体验更契合,能够快速、长期、大量地收集到相关的不良反应数据。

此外,区别于一般的平台类APP, ePConnect™能提供更高的数据质量标准,符合FDA和CDISC的相关标准,收集的相关数据能成为RWD,HEOR等研究的有效依据来源之一。

和铂医药药物警戒总监蓝丽丽女士指出:“ePConnect™-AE不仅很好地满足了法规的要求,还可以提高患者的依从性,从而保障药物治疗的疗效。在场景应用方面可以很好的整合到医药企业AE收集的不同项目中,有非常广阔的应用前景。“

关于捷信医药
上海捷信医药科技股份有限公司是医药行业数字化患者解决方案提供商。我们有超过横跨40个疾病领域,200个临床研究的行业经验,与150多个中心建立紧密合作关系。 我们帮助了25个新药的加速获批和上市,也帮助超过20000名患者联结希望。2015年底,捷信医药登录新三板。
捷信医药的解决方案包括行业知名的患者招募(信募™),中国的ePRO全套解决方案 (ePData™),还有专门为药企、医生和患者的疾病管理提供ePRO技术驱动的数字化支持解决方案(ePConnect™)。
捷信医药是国家高新技术企业,拥有数十个软件著作权,通过ISO9001,ISO27001和ISO20001等多个质量体系认证,并通过美国FDA CFR Title 21 Part 11标准的国际第三方验证。





